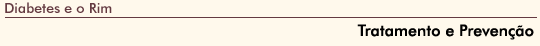  FIGURA 12-17 FIGURA 12-17
Tratamento e prevençăo da nefropatia diabética. O esteio da prevençăo é um rígido controle do açúcar no sangue e controle da hipertensăo. O Diabetes Control and Complications Trial Research Group demonstrou claramente que o controle do açúcar no sangue é muito benéfico na prevençăo tanto do início como da progressăo da nefropatia diabética [22]. Isto é inteiramente consistente com as informaçőes apresentadas nas Figuras 12-10 a 12-15, que sugerem que a hiperglicemia pode ser o mecanismo predominante que leva ŕ ativaçăo dos outros mecanismos propostos. Além disto, muitos estudos indicaram claramente que a hipertensăo predispőe ŕ e também agrava a nefropatia diabética [23]. Portanto, antes que a microalbuminúria tenha se desenvolvido, todos os pacientes devem ser estimulados a monitorar rigorosamente o açúcar no sangue e a controlar a pressăo arterial. A recomendaçăo atual é ter uma meta de pressăo arterial menor que 135/85 [23].
Quando a microalbuminúria se desenvolve, as principais terapias săo aquelas aqui mostradas. Além do rígido controle da glicemia e do controle da hipertensăo, todos os pacientes deverăo estar tomando um inibidor da enzima conversora da angiotensina (I-ECA). Os fármacos I-ECA, embora năo sejam uma cura, demonstraram claramente que desaceleram a progressăo da nefropatia diabética. Estes fármacos reduzem os níveis de angiotensina II. Uma reduçăo na angiotensina II leva a uma diminuiçăo na filtraçăo glomerular e a uma reduçăo na pressăo glomerular. Além de suas propriedades vasoativas, a angiotensina II é também um fator de crescimento. Portanto, foi proposto que os fármacos I-ECA também funcionam por inibir os efeitos promotores de crescimento da angiotensina II [24]. Os bloqueadores do receptor da angiotensina II (eg, Valsartan e Losartan), estăo agora disponíveis. Os estudos mostraram que os bloqueadores do receptor da angiotensina (ARB) săo eficazes na nefropatia diabética tipo 2 [30-32]. Os fármacos bloqueadores do receptor da angiotensina II săo especialmente úteis em pacientes que desenvolvem uma tosse enquanto estăo tomando I-ECA. Além disto, por motivos desconhecidos, a hipercalemia que pode ocorrer em pacientes que tomam I-ECA é bem menos comum em pacientes que tomam bloqueadores do receptor da angiotensina II. Outros tratamentos recomendados săo adesăo a uma dieta pobre em proteína e controle de lípides. Uma dieta pobre em proteína provavelmente age similarmente ao I-ECA, diminuindo a pressăo intraglomerular. Em termos práticos, é um pouco difícil obter uma ingestăo suficientemente baixa de proteína, porque a dieta é um tanto insípida. Ainda assim, recomenda-se que seja feito um aconselhamento dietético tanto para o controle de açúcar no sangue como para a baixa ingestăo de proteína para que os pacientes năo ingiram uma dieta rica em proteína que possa potencialmente acelerar a progressăo da doença renal. Quando os pacientes estăo se aproximando da doença renal em estágio final, é importante que a ingestăo de proteína seja liberalizada porque, neste ponto, a dieta pobre em proteína traz poucos benefícios e o risco de desnutriçăo é significativo.
 FIGURA 12-18 FIGURA 12-18
Agentes anti-hipertensivos. Além de modificaçőes na dieta e fármacos inibidores da enzima conversora da angiotensina (I-ECA), outros agentes anti-hipertensivos desempenham papéis importantes no tratamento da hipertensăo na nefropatia diabética. De particular interesse săo os bloqueadores do canal de cálcio. Especificamente, os bloqueadores de canal de cálcio năo-diidropiridina (eg, diltiazem e verapamil) oferecem benefícios na reduçăo da pressăo arterial e na reduçăo da velocidade de progressăo da doença renal, que săo semelhantes ŕqueles fornecidos pelos fármacos I-ECA [25]. Os bloqueadores do canal de cálcio (CCB) ŕ base de diidropiridina (eg, nifedipina e amlodipina) também săo úteis no tratamento da hipertensăo, mas, sozinhos, năo oferecem os mesmos efeitos sobre a desaceleraçăo da progressăo da doença renal que é observada com os fármacos I-ECA e as năo-diidropiridinas. Várias associaçőes de agentes anti-hipertensivos também foram avaliados e podem oferecer benefícios adicionais. Uma associaçăo de năo-diidropiridina e I-ECA pode ser mais efetiva que qualquer um dos fármacos sozinho em desacelerar a progressăo da nefropatia diabética [26]. Outros agentes anti-hipertensivos também podem ser usados em pacientes com nefropatia diabética, como diuréticos, b-bloqueadores e vasodilatadores, mas usados isoladamente, podem năo ter os mesmos efeitos sobre a nefropatia diabética que o I-ECA e as năo-diidropiridinas. AII — angiotensina II.  FIGURA 12-19 FIGURA 12-19
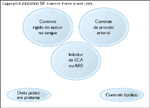
Estimativas de sobrevida para pacientes em diálise. Como observado na Figura 12-1, a nefropatia diabética é a principal causa de doença renal em estágio final (DREF) nos Estados Unidos. Além disto, a taxa de aumento em DREF resultante de diabetes é significativamente maior que a de outras principais causas de insuficięncia renal. A maior parte deste aumento reflete uma populaçăo em envelhecimento na qual o diabetes mellitus (DM) tipo 2 é prevalente. Uma revisăo cobre os problemas gerais da DREF na populaçăo diabética [27]. Provavelmente por causa das muitas afecçőes comórbidas que estăo presentes em pacientes diabéticos, os pacientes diabéticos em diálise (A) ou pós-transplante (B) tęm uma menor taxa de sobrevida que os pacientes năo-diabéticos com DREF [27]. Năo se sabe se o modo de diálise tem quaisquer efeitos, positivos ou negativos, sobre a morbidade ou mortalidade, embora a maioria dos pacientes diabéticos com DREF seja tratada por hemodiálise [27]. A decisăo de se usar hemodiálise versus diálise peritoneal deve ser tomada levando-se em consideraçăo fatores como estilo de vida, saúde geral do paciente e afecçőes comórbidas (eg, comprometimento da visăo). O uso de diálise peritoneal pode simplificar ou complicar o controle da glicose. O dialisato peritoneal contém concentraçőes variáveis de glicose (1,5%; 2,5% e 4,25%) e, por este motivo, o controle da glicose pode ser significativamente afetado quando ocorrem as trocas do dialisato. Este problema é minimizado injetando-se insulina diretamente na soluçăo do dialisato. Este método de aplicaçăo de insulina pode ser usado năo apenas para contrabalançar os efeitos da exposiçăo aguda a altas concentraçőes de glicose, mas também como um meio de se fornecer um nível constante de insulina que pode ajudar na manutençăo de uma glicemia razoavelmente estável durante todo o dia. Este método de aplicaçăo de insulina é eficaz para a manutençăo global da glicemia apenas para pacientes que fazem trocas de fluido durante o dia. Muitos pacientes preferem fazer diálise peritoneal por repetidas trocas noturnas, utilizando uma máquina que cicla o fluido para dentro e fora do abdômen. Durante o dia, estes pacientes năo tęm trocas de fluido. A insulina injetada em cada bolsa ŕ noite é dosada para manter uma concentraçăo estável de glicose durante toda a noite e o paciente segue um esquema padronizado de injeçőes subcutâneas durante todo o dia. (Dados de U. S. Renal Data System [28].)
 FIGURA 12-20 FIGURA 12-20
Transplante de rim e pâncreas. Acredita-se que o transplante de rim ou de rim/pâncreas seja a terapia preferencial para pacientes com doença renal em estágio final. Os índices de sobrevida após transplante săo maiores que aqueles para pacientes que permanecem em diálise (veja a Fig. 12-19). A nefropatia diabética recidiva na maioria dos receptores de transplante de rim, embora isso geralmente ocorra muitos anos depois que a nefropatia diabética for grave o bastante para causar perda do transplante (A a D). A perda do transplante por causa da recidiva de nefropatia diabética é, portanto, rara.
O transplante de pâncreas é feito somente em conjunçăo com um transplante de rim. Tem sido uma crença que, por poder os níveis de glicose no sangue ser controlados com a insulina, o transplante de pâncreas ofereça riscos demais em comparaçăo com seus benefícios. Os maiores riscos estăo relacionados ŕ imunossupressăo e ao maior risco de infecçőes que ameaçam a vida. Além disto, há poucas evidęncias mostrando que um transplante precoce de pâncreas afetaria a progressăo da nefropatia diabética. Um intrigante estudo de Fioretto et al. [29] mostra, porém, que o transplante isolado de pâncreas pode causar uma verdadeira reversăo das lesőes da nefropatia diabética, que se torna evidente somente após 5 anos de normoglicemia. Este achado pode aumentar o interesse pelo transplante de pâncreas como uma maneira de prevenir o desenvolvimento da nefropatia diabética. (Adaptado de Fioretto et al. [29].)  FIGURA 12-21 FIGURA 12-21
Recomendaçőes de triagem e tratamento para proteinúria. As recomendaçőes atuais para o tratamento de proteinúria no Joslin Diabetes Center, em Boston, Massachusetts, se baseiam no nível de proteinúria. Os médicos do Joslin Diabetes Center acreditam que um modelo colaborativo de assistęncia é melhor para o paciente com diabetes. Portanto, pacientes com nefropatia diabética inicial săo assistidos primariamente por um endocrinologista em consulta com um nefrologista. Quando os pacientes se aproximam da doença renal em estágio final, boa parte da assistęncia ao paciente é transferida ao nefrologista, mas outros prestadores de assistęncia (eg, endocrinologista, oftalmologista, nutricionista) continuam a trabalhar em colaboraçăo para assistir o paciente. ECA — enzima conversora da angiotensina; PAM — pressăo arterial média.
voltar |